Fälschungsrichtlinien für Arzneimittel – Medikamentenfälschung verhindern
Medikamentensicherheit ist ein hohes Gut, das durch gefälschte Medikamente immer wieder in Gefahr gebracht wird. Hinter gefälschten Medikamenten können sich Arzneien mit falsch deklarierten, verdünnten oder fehlenden Inhaltsstoffen verbergen. Durch täuschend echte Verpackung oder eine Neuverpackung in Originalschachteln werden Händler und Patienten über den tatsächlichen Inhalt irregeleitet.
In der Regel werden Fälschungen erheblich billiger hergestellt und verkauft als die echten Präparate. Weltweit, so eine Schätzung der amerikanischen FDA (Food and Drug Administration), sollen über 10 % aller im Umlauf befindlichen Medikamente gefälscht sein. Die möglichen Folgen: Patienten nehmen im Glauben, es mit richtigen Medikamenten zu tun zu haben, unwissentlich unwirksame oder gar schädliche Stoffe ein, mit möglicherweise drastischen Folgen für ihre Gesundheit.
Ehrliche Pharmaproduzenten müssen nicht nur Umsatzeinbußen aufgrund der gefälschten Billigkonkurrenz hinnehmen, sondern auch Vertrauensverluste bei den Verbrauchern, die sich getäuscht fühlen. Die von der Weltgesundheitsorganisation geforderten Fälschungsrichtlinien für Arzneimittel, die viele Staaten eingeführt haben, sollen die Gesundheit der Patienten schützen. Daher liegt die Einhaltung der Vorschriften im Interesse aller seriösen Pharmahersteller.
Sie benötigen weitere Informationen zu globalen Fälschungsrichtlinien? Wir beraten Sie gerne!
Wir informieren Sie auf dieser Seite über die globalen Fälschungsrichtlinien für Arzneimittel:
- Weltweiter Überblick
- Europa (2011/62/EU )
- USA (DSCSA)
- Südafrika
- Russland (Gesetz 61-FZ)
- Brasilien (SNCM)
- Umsetzung der Fälschungsrichtlinie
Fälschungsrichtlinien weltweit – ein Überblick
Overview of falsification guidelines worldwide
Den Gefahren gefälschter Medikamente für Verbraucher und Unternehmen sind die Gesetzgeber auf der ganzen Welt durch den Erlass nationaler und supranationaler Fälschungsrichtlinien entschlossen entgegengetreten. Durch die Einhaltung der entsprechenden Vorschriften können Pharmahersteller und Verpackungsdienstleister sicher sein, dass sie ihre Produkte in den Zielmärkten problemlos vertreiben können und dass gefälschte Billigprodukte zuverlässig aus diesen Märkten entfernt werden.
Weltweit gibt es mehrere Fälschungsrichtlinien in verschiedenen Stadien der Umsetzung, die zum Teil unterschiedliche Anforderungen stellen. In dieser Übersicht erfahren Sie, wo die Gemeinsamkeiten und Besonderheiten liegen.
- Codierung
- Tamper-Evident Verschluss
- Aggregation
- GS1 international
Codierung: Andere Länder, andere Kennzeichnung von Arzneimitteln
Alle Fälschungsrichtlinien verlangen eine individuelle Produkt-Identifikationsnummer auf den Medikamenten. Hinzu kommen beim Großteil der Richtlinien das Verfallsdatum für das Medikament, sowie eine Chargennummer und gegebenenfalls eine Seriennummer. In welchem Format diese Kennzeichnungen jedoch erfolgen, kann stark variieren. Immer enthalten sein muss aber menschenlesbare Klarschrift, sowie ein maschinenlesbarer Barcode. Ähnliches trifft auf die Art der Produkt-Identifikationsnummer zu – häufig wird das GTIN-Format der GS1 verlangt, hin und wieder wird auch eine ID-Nummer im NTIN oder länderspezifischen Formaten vorgegeben (wie z. B. PPN in Deutschland, CIP in Frankreich, KDC in Korea, CNK in Belgien, AIC in Italien usw.). In der Produkt-Identifikationsnummer sind üblicherweise folgende Informationen enthalten: Ein Länder-Präfix, die Unternehmensnummer, die Artikelnummer und eine Prüfziffer.
Tamper-Evident Verschluss: Besonderheit der EU-Fälschungsrichtlinie
Der Tamper-Evident-Verschluss wird bei verschreibungspflichtigen Medikamenten in Ländern verlangt, die im Geltungsbereich der am 9. Februar 2019 in Kraft getretenen EU-Richtlinie über gefälschte Arzneimittel liegen. Das Siegel verhindert eine nachträgliche Manipulation des verpackten Medikamentes oder ein Verbergen gefälschter Medikamente in Originalverpackungen. Ist das Siegel beim Verkauf beschädigt oder geöffnet, darf eine Abgabe an den Kunden nicht erfolgen.
Die Lösung für den manipulationssicheren Verschluss von Medikamentenschachteln:
Aggregation: Track & Trace über die gesamte Lieferkette hinweg
Eine Aggregation, die die Nachvollziehbarkeit einer einzelnen Produktverpackung über den gesamten Transportweg und mehrere Verpackungsebenen hinweg erlaubt, wird nur von manchen Richtlinien gefordert, z. B. in Russland oder in der Türkei. Länder wie die USA behalten sich die Entscheidung noch vor, in der EU und einigen anderen Ländern ist die Aggregation freiwillig. In Brasilien muss ab dem Jahr 2021 jede Einzelschachtel über die verschiedenen Aggregationsstufen hinweg nachvollziehbar sein. Auch hier kann die Art der Codierung je nach Land unterschiedlich ausfallen. Obwohl die Aggregation in einigen Fälschungsrichtlinien – wie eben der europäischen – rein juristisch freiwillig ist, kann sie doch von Kunden wie Großhändlern und Krankenhausapotheken erwünscht sein. Diese nehmen zum Teil große Lieferungen in Paket- oder Palettengröße entgegen – die Möglichkeit zur Verifizierung einer kompletten Lieferung direkt am Wareneingang erleichtert ihnen den Warenfluss erheblich.
Mit unseren Aggregations-Lösungen TQS-CP und TQS-CP Bottle stellen Sie Ihren Kunden genau das zur Verfügung: Auf Paket- und Palettenebene verifizierbare Medikamente. Der Bediener befüllt den Umkarton lagenweise. Nach jeder Lage erfasst die integrierte Kamera die Codes der Medikamentenschachteln. Wenn der Karton befüllt und die Aggregationsstufe abgeschlossen ist, erstellt die TQS-CP automatisch das richtige Etikett. Dies funktioniert auf mehreren Aggregationsstufen.
GS1 international – Wächterin über die Identifikationsnummern
Die in Brüssel ansässige GS1 international gestaltet die globalen Standards für verschiedene Branchen und vergibt die Global Trade Item Numbers (GTIN), sowie weitere Identifikationsnummern für Medikamente. Sie gewährleistet die internationale Verständigung über standardisierte Barcodes und Identifikationsnummern. Dank der engen Zusammenarbeit von Wipotec mit GS1 Germany und der GS1 Global Healthcare User Group geben wir Neuerungen rasch an unsere Kunden weiter und setzen relevante Vorgaben direkt um.
Europas Falsified Medicines Directive: Die Fälschungsrichtlinie 2011/62/EU und was sie für Hersteller in der EU bedeutet
2011 wurde die EU-Fälschungsrichtlinie 2011/62/EU veröffentlicht. Sie gilt seit Februar 2019 für alle verschreibungspflichtigen sowie bestimmte rezeptfreie Arzneimittel in der Europäischen Union. Auch die Nicht-EU-Staaten Island und Norwegen unterliegen der europäischen Fälschungsrichtlinie. Italien, Belgien und Griechenland serialisierten bereits vor Februar 2019. Jedoch nicht gemäß der EU-Richtlinie, sondern unter Zuhilfenahme von Vignetten oder Bollini. Sie haben weitere sechs Jahre Zeit, die EU-Richtlinien vollständig umzusetzen.
Medikamente, die nicht die gemäß der EU-Richtlinie zu gefälschten Arzneimitteln (EU Falsified Medicines Directive) notwendigen Sicherheitsmerkmale tragen, dürfen in der EU nicht mehr vertrieben werden.
In der Praxis wird die Einzelverpackung bei der Abgabe an den Patienten durch den Apotheker abgescannt. Liefert der Scan eine Fehlermeldung, darf das Medikament nicht ausgegeben werden.
Sie benötigen weitere Informationen zur EU-FMD oder wünschen ein Beratungsgespräch?
- Produkt-Identifikationsnummer, im Format GTIN, NTIN (oder PPN für Deutschland)
- Chargennummer
- Verfallsdatum
- Individuelle Seriennummer der Einzelverpackung
- Ggf. nationale Produktnummern für Erstattungszwecke durch nationale Kassen (national healthcare reimbursement number, NHRN)
Darüber hinaus müssen Einzelverpackungen mit einem intakten Tamper-Evident Siegel vor Manipulation geschützt sein.
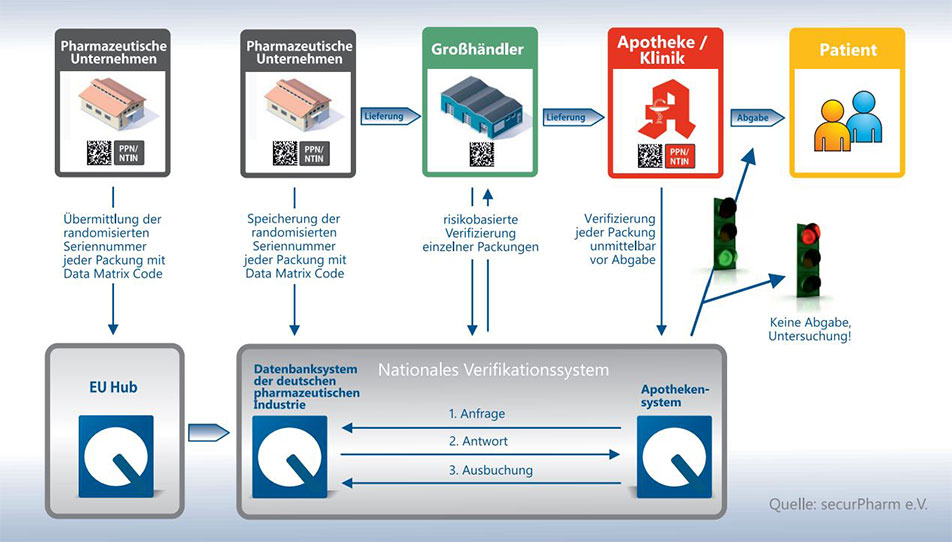
securPharm: Nationales Verifikationssystem
securPharm: Nationales Verifikationssystem gewährleistet sichere Arzneimittel in Deutschland
Sobald eine Medikamentenpackung in der Apotheke abgescannt wird, wird der eingelesene Code mit einer Online-Datenbank abgeglichen, um zu verifizieren, dass es sich um ein legales, sicheres Arzneimittel handelt. Die europäischen Staaten haben jeweils nationale Systeme in der jeweiligen Landessprache aufgebaut, in dem die entsprechenden Daten hinterlegt sind. In Deutschland läuft das System unter dem Namen securPharm. Die davor in Deutschland übliche, meist in einem Strichcode codierte Pharmazentralnummer (PZN) wurde mit Einführung von securPharm in die von der europäischen Fälschungsschutzrichtlinie vorgeschriebene Produkt-Identifikationsnummer (NTIN bzw. PPN) aufgenommen. Sie wird gemeinsam mit den anderen erforderlichen Informationen im 2D Matrixcode festgehalten.
Quelle: securPharm e.V.: „Regeln zur Codierung verifizierungspflichtiger Arzneimittel im deutschen Markt“
European Medicines Verification Organisation (EMVO)
Mit Hilfe der EMVO Medikamente EU-weit identifizieren
Die nationalen Datenbanken werden seit 2015 in einem europäischen Knotenpunkt zusammengefasst. Dies gewährleistet die europaweite Vergleichbarkeit der Daten und ermöglicht so den europäischen Binnenhandel für sichere Pharmaprodukte. Dieser EU-Hub steht unter der Obhut der European Medicines Verification Organisation, kurz EMVO, die das Projekt weiter ausbaut und betreibt. Hersteller von Pharmaprodukten speisen die benötigten Daten direkt in die europäische Datenbank ein, die ihrerseits mit den nationalen Datenbanken kommuniziert. Der Aufbau der nationalen und internationalen Datenbanken wurde 2019 rechtzeitig zum Inkrafttreten der Europäischen Fälschungsrichtlinie abgeschlossen.
DSCSA – der Drug Supply Chain Security Act sorgt für sichere Arzneimittel in den USA
Die US-amerikanische Fälschungsrichtlinie DSCSA ist Teil des DQSA (Drug Quality Security Act) der FDA. Sie wurde im Jahr 2013 vom Präsidenten unterzeichnet und soll bis 2023 vollständig umgesetzt sein. Bereits seit 2015 sind Hersteller und Händler von verschreibungspflichtigen bzw. erstattungsfähigen Medikamenten verpflichtet, die notwendigen Informationen auf Chargen-Ebene zur Verfügung zu stellen und alle Transaktionsdaten bis hin zur schlussendlichen Ausgabe in der Apotheke festzuhalten. Durch die lückenlose Nachvollziehbarkeit der Chargennummern von Arzneimitteln können nicht nur gefälschte, sondern auch gestohlene Medikamentenchargen rasch erkannt und sichergestellt werden. Hierbei gelten für die verschiedenen Stakeholder, Produzenten, Verpackungsdienstleister, Großhändler und Verkäufer gestaffelte Fristen. Ab November 2023 wird die Pflicht auf die Kennzeichnung von Arzneimittel-Einzelpackungen ausgeweitet. Die Übergangsfrist für die Kennzeichnung von Einzelverpackungen begann im November 2018. Entsprechende Vorschriften galten zuvor in einzelnen US-Bundesstaaten. Diese wurden dann durch die US-weite Regelung ersetzt.
Sie benötigen weitere Informationen zur DSCSA oder wünschen ein Beratungsgespräch?
Diese Angaben verlangt der DSCSA
Folgende Informationen müssen ab November 2018 in Form eines 2D Matrix-Codes und in Klarschrift auf jeder Einzelverpackung angegeben sein:
- Nationale Produkt-Identifikationsnummer im GTIN-Format
- Individuelle Seriennummer der Einzelpackung
- Verfallsdatum des Medikaments
- Chargenbezeichnung des Arzneimittels
Serialisierung von HDPE-Flaschen
Serialisierung von HDPE-Flaschen in den USA
Hersteller und Verpacker für den US-amerikanischen Markt stehen neben der Umsetzung der DSCSA-Richtlinie vor einer weiteren Herausforderung: Die in den USA handelsüblichen HDPE-Flaschen für Tabletten und Kapseln. Im Gegensatz zu den in Europa geläufigen Faltschachteln mit Blisterpacks stellen diese ganz andere Anforderungen an die Herstellerlogistik. Dazu gehören auch die sogenannten Helper-Codes oder Hilfscodes. Sie werden zur Aggregation von Flaschen zu größeren Bündeln auf Deckel oder Boden der Flaschen angebracht. Dies kann auch „unsichtbar“, mit UV-Tinte geschehen. Der Helper-Code ermöglicht die Identifikation der Verpackungen, selbst wenn die individuellen Flaschenetiketten durch die Bündelung nicht mehr lesbar sind.
Die Bottle-Serie von Wipotec bedruckt und inspiziert Flaschen und Vials zuverlässig. Finden Sie Ihre Lösung zur Produktinspektion, zuverlässigen Serialisierung und semiautomatischen Aggregation von Flaschen und Vials, um den Anforderungen der amerikanischen Fälschungsrichtlinie DSCSA gerecht zu werden.
Ultraschnelle Runduminspektion – kompakte Serialisierung – Semiautomatische Aggregation – Druck von Helper-Codes
Arzneimittelkennzeichnung mit E-Pedigree
US-weite Rückverfolgbarkeit der Arzneimittelkennzeichnung mit E-Pedigree
E-Pedigree ist gewissermaßen das amerikanische Pendant zum europäischen EMV-System. In diesem „elektronischen Stammbaum“ sind alle Daten eines Präparates hinterlegt, inklusive der Transaktionsdaten, die entlang der Lieferkette eines Pharmaproduktes erhoben werden. Auch hier gibt es kleinräumigere Datenbanken auf Ebene der Bundesstaaten, die in einer internationalen Datenbank zusammengefasst werden. Viele der bundesstaatlichen Datenbanken basieren auf dem System des Vorreiters Florida, der E-Pedigree bereits 2005 einführte.
Fälschungsrichtlinie in Südafrika: Serialisierung der Sekundär- und Tertiärverpackungen
Gesetz 61-FZ: Einführung einer Fälschungsrichtlinie in Russland
Medikamentenfälschung und Schattenwirtschaft sind in Russland ein gravierendes Problem. In Reaktion darauf erließ die Duma 2010 das Gesetz 61-FZ zum Medikamentenhandel, das zur Steigerung der Medikamentensicherheit beitragen soll. Bis Ende 2017 lief ein auf einige essentielle Wirkstoffe beschränktes Pilotprojekt, das Herstellung und Lieferkette von Pharma-Produkten überwachte, die im Raum Moskau und St. Petersburg über den Ladentisch gingen. Das Ziel war es, gefälschte Medikamente zuverlässig zu erkennen. Seit Januar 2020 sollen alle verschreibungspflichtigen Medikamente serialisiert und aggregiert werden.
Fälschungsrichtlinie für Medikamente in Brasilien: Track & Trace mit SNCM
Einen Schritt weiter ist die brasilianische Gesundheitsbehörde ANVISA. Im Jahr 2014 erließ sie die SNCM abgekürzten Regelungen für ein Track & Trace-System, mit dem Herstellung und Lieferkette von Medikamenten überwacht werden. Ähnlich wie bei den europäischen und amerikanischen Systemen sollen auch hier Produktidentifikationsnummer, Seriennummer, Chargennummer und Verfallsdatum der Medikamente auf den Verpackungen aufgedruckt werden. Nach einigen Verspätungen in der Umsetzung gibt die momentan gültige Regelung den 1. April 2022 als Frist für die umfassende Implementierung des „Sistema Nacional de Controle de Medicamentos“ an.

Südafrika hat sich dem weltweiten Kampf gegen Arzneimittelfälschungen angeschlossen. Die Pharma-Exporte aus der EU nach Südafrika haben pro Jahr einen Wert, der eine Milliarde Euro übersteigt. Das macht die Kodierungs- und Serialisierungsrichtlinien in Südafrika zu einer bedeutenden Umstellung für europäische Pharmahersteller. Die Unternehmen, die nach Südafrika liefern, müssen eine Neuordnung ihres Verpackungsprozesses vornehmen, um den Anforderungen gerecht zu werden. Die Serialisierung der Sekundär- und Tertiärverpackung soll bis 2022 durchgeführt werden. Die schrittweise Umsetzung der Verordnung soll den Pharmaunternehmen genügend Zeit zur Vorbereitung geben.
Umsetzung der Fälschungsrichtlinien – wie gelingt das Verpackern und Pharmaprofis?
Die Umsetzung der nationalen und internationalen Fälschungsrichtlinien stellt Pharmahersteller und Verpackungsdienstleister vor große Herausforderungen. Diese betreffen die technische Seite, aber auch die Mentalität im jeweiligen Unternehmen. Wipotec kann Ihnen mit passgenauen Lösungen und vielfältigen Informationen helfen, diese Hürden zu meistern. Vor allen Dingen die Auflage, nicht mehr nur jede Charge, sondern jede einzelne Verpackung individuell zu kennzeichnen, macht oftmals Umstellungen in der Produktionslinie und Neuanschaffungen notwendig. Hersteller und Verpacker sehen sich daher einer Reihe von Herausforderungen gegenüber.
Handeln in der Führungsebene
Die Einhaltung von Vorschriften erfordert effektive Zusammenarbeit
In der Realität vieler Betriebe stellen wir fest, dass die Umstellung in der Produktionslinie vielerorts mehr als „nur“ ein technisches Problem ist, das der Fertigungsleiter im Alleingang regeln kann. Um die perfekte Lösung zu finden, die zu den Anforderungen der Zielländer ebenso passt wie zu den Bedingungen im eigenen Unternehmen, sind oft Gespräche mit mehreren Lösungs-Anbietern notwendig. Lohnhersteller müssen sich frühzeitig mit ihren Auftraggebern und Partnern in Verbindung setzen, denn das Finden der besten Lösung nimmt oft Zeit in Anspruch. Die Herausforderung besteht darin, die extrem hohe Priorität dieser Fragestellungen zu erkennen und rechtzeitig ausreichend Zeit für ihre Klärung einzuräumen. Mehrere Aufgaben müssen gleichzeitig angegangen werden – dies sind nicht nur variable Lösungen für die Codierung und Kennzeichnung von Verpackungen und Chargen, sondern auch die Datenverarbeitung und -übermittlung an die nationalen Datenbanken.
Die Lösungen von Wipotec bieten hier einen entscheidenden Vorteil: Dank der offenen Schnittstellen unserer Maschinen ist eine Kompatibilität mit Softwarelösungen mehrerer Level 3 Dienstleister gegeben.
Erfahren Sie mehr über die Vorteile der offenen XML-Schnittstellen!
Sie können nicht länger warten? Die TQS Fast Track ist die schnelle Plug-and-Play Lösung für voll automatisierte Serialisierung innerhalb von 6 Wochen!
Druckqualität und Datenmanagement
Anforderungen an Druckqualität und Datenmanagement erfordern Investitionen
Der anfallende Investitionsaufwand für das Finden, Beschaffen und Integrieren der geeigneten Lösungen sollte ebenfalls nicht unterschätzt werden. Das Bedrucken von Verpackungen mit langlebigen, hochauflösenden Codes und Beschriftungen, deren Maschinenlesbarkeit stets gegeben ist, ist keine kleine Herausforderung. Die hohen Geschwindigkeiten machen den Einsatz geeigneter Produkttransport-Technologien notwendig, um ein Verwischen des Drucks zu vermeiden. Auch Lichtechtheit und Abriebfestigkeit des Drucks müssen auf verschiedenen Untergründen gewährleistet sein, um die Lesbarkeit der Codierungen während der gesamten Lebensdauer des Produkts zu garantieren. Nur durch ein hohes Maß an Übereinstimmung kann ein Ausmustern von Produkten durch die Bilderkennungssysteme vermieden werden. Besonders bei kleinen Codes mit hoher Dichte sind geeignete Druck- und Produkttransportsysteme unumgänglich um die notwendige Kennzeichnungsqualität bei hoher Druckgeschwindigkeit zu gewährleisten.
Um eine Compliance mit den Fälschungsrichtlinien zu gewährleisten, sollten Pharmahersteller und Verpackungsdienstleister nicht am falschen Ende sparen. Der ROI ist fortgesetzte Marktfähigkeit.
Flexibilität
Ein internationaler Markt erfordert ein hohes Maß an Flexibilität
Hersteller, die von einem Werk aus mehrere Regionen beliefern, müssen die nötige Flexibilität für unterschiedliche Formate und Drucklayouts mitbringen. Das bedeutet auch, dass die Verpackungslinie und ihre Druckereinheiten schnell und fehlerfrei auf die jeweiligen Fälschungsrichtlinien umgestellt werden können. Die Hersteller müssen dafür den individuellen Datensatz für jedes Einzelprodukt erstellen und anschließend in das jeweilige nationale oder internationale Datenbanksystem laden. Die leicht zu bedienenden Benutzeroberflächen der Lösungen von Wipotec mit der Softwarefunktion ConfigureFast ermöglichen die rasche und fehlerfreie Einstellung länderspezifischer Codes ohne Verzögerung im Betriebsablauf. Die flexible Software ermöglicht den unkomplizierten Codewechsel. Der integrierte LineManager hält alle Produktionsdaten zunächst in im lokalen Zwischenspeicher fest und übermittelt sie weiter an das angeschlossene Level 3 System. Der temporäre Speicher sichert Ihre Daten gegen Verlust bei Stromausfällen und anderen Unwägbarkeiten
Kompakte Lösungen bei wenig Platz: Track & Trace auf dem Fast Track
In den Herstellungs- und Verpackungslinien von Pharmaherstellern und Lohnverpackern ist freier Platz oft Mangelware. Die sehr kompakten Maschinen von Wipotec erleichtern die Integration wichtiger Funktionen in die bestehenden Linien auf minimalem Raum. Das Beste: Mit unseren Fast Track Lösungen steht Ihre Serialisierung innerhalb von nur 6 Wochen.
Die TQS-SP ermöglicht die Serialisierung und Tamper-Evident-Etikettierungen einzelner Medikamentenpackungen auf kleinstem Raum. Mit der TQS-HC-A mit Tamper Evident erfüllen Sie drei Aufgaben auf 1800 mm Länge vollautomatisch: Kontrollwiegen, Serialisieren und Etikettieren.
Ihre Vorteile:
- Zuverlässige Compliance mit internationalen Fälschungsrichtlinien
- Auch bei wenig verfügbarem Raum
- Lösung innerhalb von sechs Wochen nach Bestellung
- Modular, skalierbar und unkompliziert in bestehende Linien integrierbar
Informieren Sie sich jetzt über die kompaktesten Serialisierungslösungen für den EU-Markt!
Darum lohnt es sich, sich auf Chancen statt auf Herausforderungen zu konzentrieren
It’s worth seeing the international falsification directives as an opportunity to optimise your business performance and contribute to patient protection.
- Full compliance with the FMD will guarantee your continued marketability.
- You’ll be one step ahead of your competitors due to your flexibility with our solutions.
- The traceability of products required by the falsification directives will provide you with valuable Track & Trace data on the efficiency of your supply chain and sales – allowing you to control and optimise your operations.
Find the right solution for your application now!
Successful solutions for the pharmaceutical industry: Find out more about customer projects with Wipotec.



![[Bitte in "Deutsch" übersetzen:] TQS-CP for semi-automatic aggregation of drugs [Bitte in "Deutsch" übersetzen:] TQS-CP drug aggregation](/fileadmin/wipotec-ocs/en/applications/serialisation-pharma/Falsified-medicines-directives/tqs-cp-aggregation-drugs.jpg)


![[Bitte in "Deutsch" übersetzen:] Product identification number PPN [Bitte in "Deutsch" übersetzen:] Product identification number PPN](/fileadmin/wipotec-ocs/en/applications/serialisation-pharma/Falsified-medicines-directives/pharmaceutical-product-identification-number-ppn.jpg)

![[Bitte in "Deutsch" übersetzen:] TQS-SP: User-friendly serialisation in the smallest of spaces [Bitte in "Deutsch" übersetzen:] TQS-SP: User-friendly serialisation](/fileadmin/wipotec-ocs/en/applications/serialisation-pharma/Falsified-medicines-directives/tqs-sp-user-friendly-serialisation.jpg)
![[Bitte in "Deutsch" übersetzen:] TQS-HC-A: Serialisation, weight inspection and tamper-evident [Bitte in "Deutsch" übersetzen:] TQS-HC-A: Serialisation, weight inspection, tamper-evident](/fileadmin/wipotec-ocs/en/applications/serialisation-pharma/Falsified-medicines-directives/tqs-hc-a-tamper-evident.jpg)